シストランス異性体って?【化学】【高校】
皆さんこんにちは!
今回はシス・トランス異性体(幾何異性体)について解説していきます!
有機化学の割と序盤で習うとは思いますがいったい何なのかというところを詳しく簡単に話していければなと思います!

そもそも異性体って?
まず異性体とは何なのかよくわかりません!という人も多いと思います。
一言で言うと
「組成式が一緒なのに構造が異なるやつら」のことです。
例えば、アルカンの一種であるは、炭素が4個と水素が10個でできています。
次のような2種類の構造が考えられます。
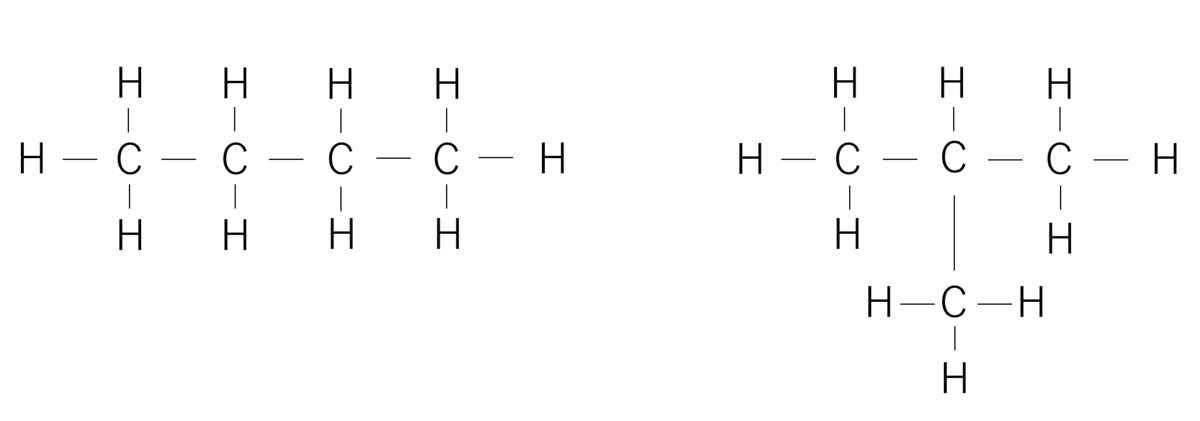
原子の数を数えると炭素4個、水素10個になっていますね!
どちらもであるといえます。
このように同じ組成式()でありながら構造が異なることを構造異性体といいます。
それではそのなかでもシストランス異性体とは何なのかについて説明していきます。
シストランス異性体(幾何異性体)って?
二つの炭素間の二重結合によって生まれる異性体のことです。
二重結合は単結合よりも結合力が高く、開店することができません。
つまり、炭素が同一平面上に並びます。
この時立体異性体は生まれるのです。
例を見てみましょう。
は次のような構造を取ります。

一見同じじゃない?と思うと思います。
二重結合のところでくるっと回転することができれば確かに同じなのですが、二重結合は強い結合力ゆえに回転をすることができません。
なのでこの二つの構造は全く別物になるということです。
名前の付け方
「どっちがシスでどっちがトランスなのか」
先ほど例で取り上げた2-ブテンを用いて解説していきます。

メチル基()が二重結合に対して同じ側に結合しているのがシス、反対側に結合しているのがトランスです。
よって今回の例では
左がシスー2-ブテン、右がトランスー2-ブテン
と名付けられています。
ちなみにトランス(trans)は英語で「向こう側の」という意味があります。
まとめ
今回はシストランス異性体について扱いました。
○二重結合に対して同じ側に結合しているのがシス、反対側に結合しているのがトランス
どっちがどっちか見極めることができれば今回の内容は完璧です!
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
絶対値のついた方程式・不等式の解き方 その2【数学】【高校】
皆さんこんにちは!
今回は絶対値を含む方程式・不等式を扱っていきます。
下の記事の続きになっていますので先にそちらをご覧ください!
study-college-student.hatenablog.com
それでは前回の復習からスタートです!

前回の復習
k > 0としたとき、
① 方程式の解は
② 不等式の解は
③ 不等式の解は
②の場合
の意味を考えてみましょう。
前回も書いた通り絶対値とは原点からの距離のことです。
つまり、前回同様日本語に直すと次のようになります。
「変数xの原点からの距離がkよりも小さい」
この不等式はこれを意味しています。
を満たすxの範囲を求めよ。
という問題があったら、
原点からの距離がkよりも小さくなるようなⅹの範囲を求めればよいのです。
例題②
問:不等式を解け。
まずはこの式の意味を考えてみましょう。
「(x-3)の絶対値は原点との距離が4より小さい」
つまり、
(x-3)が-4と4の間であればよいということです
これを式に直すと、
これは答えではないので注意してください。
あくまで求めたいのはxの範囲なので、
辺々に3を足して、
これが答えとなります。
③の場合
ではこれは何を表しているでしょうか。
「xの絶対値はkよりも大きい」
ですよね!つまり、
不等式を解けという問題は
絶対値がkよりも大きくなるようなxの範囲を求めればよいのです。
例題③
問:不等式を解け。
(x -2)の絶対値が3よりも大きいということを表しています。
つまり、(x - 2)が3よりも大きい、もしくは-3よりも小さければ良いということです。
これを式で表すと、
もしくは、
それぞれを解いて
,
というように答えが出せます。
まとめ
前回と合わせて2回で絶対値付きの方程式や不等式の解き方を扱いました。
① 方程式の解は
② 不等式の解は
③ 不等式の解は
この三つの式をほかの人に説明できるようになっていたら完璧です!
基本的な問題のみ扱ったのでまた発展編を作ろうかなと思っています!
それでは!
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
絶対値のついた方程式・不等式の解き方【数学】【高校】
皆さんこんにちは!
今回は高校一年生の数学Iで習う絶対値のついた方程式、不等式の解き方について解説していきます。
ここは理解することが難しい範囲ですが、一緒に頑張っていきましょう!

問題は大きく3種類
絶対値付きの方程式・不等式と言われたら大きく3種類に分類することができます。
k > 0としたとき、
① 方程式の解は
② 不等式の解は
③ 不等式の解は
全ての問題に対して上の三つの公式のようなものを適用させれば答えは出せます。
それぞれについて、なぜそうなるのかという理由と例題を見ていこうかなと思います。
①の場合
方程式の解は
まずの意味から考えていきます。
この式は何を表しているのでしょうか。
日本語にすると次のようになります。
「変数xの絶対値はkです。」
復習になりますが絶対値とは数直線上での原点からの距離でした。
つまり、こう言いかえることもできます。
「変数xの原点からの距離はkです。」
を満たすxを求めよ。
という問題は、
原点からの距離がkのなるようなxの値を求めればよいということです。
例題も見ていきます。
例題①
問:方程式を解け。
この問題を考えていきましょう。
先ほどと同様に日本語に直してみると次のようになります。
「原点との距離が4であるような(x - 1)を求めよ。」
では原点との距離が4なのはどんな数字でしょう。
これは中学校で習ったと思いますが、
原点0から正の方向に4進むと+4
負の方向に4進むとー4
よって(x - 1)がになればいいということですね。
これを式にしていきます。
よって
というように答えを出すことができます。
もう1問見ていきます。
問:方程式を解け。
先ほどの問題との違いは、右辺にもxが含まれているというところです。
こういった問題は場合分けを使って解いていきましょう。
のように、
絶対値の中身が正のときはそのまま、負のときはマイナスをかけて絶対値を外します。
この考えを使います。
つまり絶対値の中身が正か負かで場合分けをします。
それでは解答に移ります。
[1]つまり
のとき
この時絶対値はそのまま外れるので、
これを解くと、
よく確認してみると、今回はの時を考えていたので、
は不適であり、解無しです。
[2]つまり
のとき
この時絶対値はマイナスをかけて外さなくてはならないので、
これはを満たすので、適しています。
[1][2]より
以上のように答えが求められます。
まとめ
今回はここまでにします!
絶対値を含む方程式の解き方について説明しました。
次回は絶対値を含んだ不等式をメインに扱っていきますのでそちらも併せてご覧ください。
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
手作り梅酒と化学の話【浸透圧】【高校】
皆さんこんにちは!
関東は梅雨ですが気温がだいぶ高くなりじめじめしてきましたよね。
そんな時期に梅ジュース(梅酒)を自分で作ってみようと考えている人も多いと思います。
なので今回は梅ジュース(梅酒)作りと化学の関係性について書いていこうと思います!

梅酒作りと浸透圧
梅酒を手作りする際に何を入れるかご存じですか?
当然、梅とお酒は入れるのですが、あともう一つ必須の材料があります。
それが、氷砂糖です。
この氷砂糖はただ甘くする目的だけで入れているわけではありません。
さらに、普通の砂糖ではいけない理由もあります。
その理由について化学の観点で話していきたいと思います。
そのために必要なキーワードが浸透圧です。
浸透圧って??
では先に浸透圧の話をしていきます。
浸透という言葉は日常でもよく使われますが、この言葉はどんな意味なのでしょう。
化学では「半透膜と呼ばれる小さな穴の開いた膜を通り、水分子が移動する現象」のことを浸透と呼びます。
このときの水分子の移動の方向が重要で、その方向は「薄い方から濃い方」です。
薄い溶液から濃い溶液の方へ水が動くとしっかり覚えてください。
大事なことなので2回言いました(笑)
図を使ってもう少し詳しく説明していきます。

今、図のようにU字型の管を半透膜で区切って、純水と薄いデンプンの溶液を入れたとします。
先ほど説明した通り浸透が起きるのですが、水分子の移動の方向は「薄い方から濃い方へ」でした。
よって今回は純水側の水分子が水溶液側に移動します。
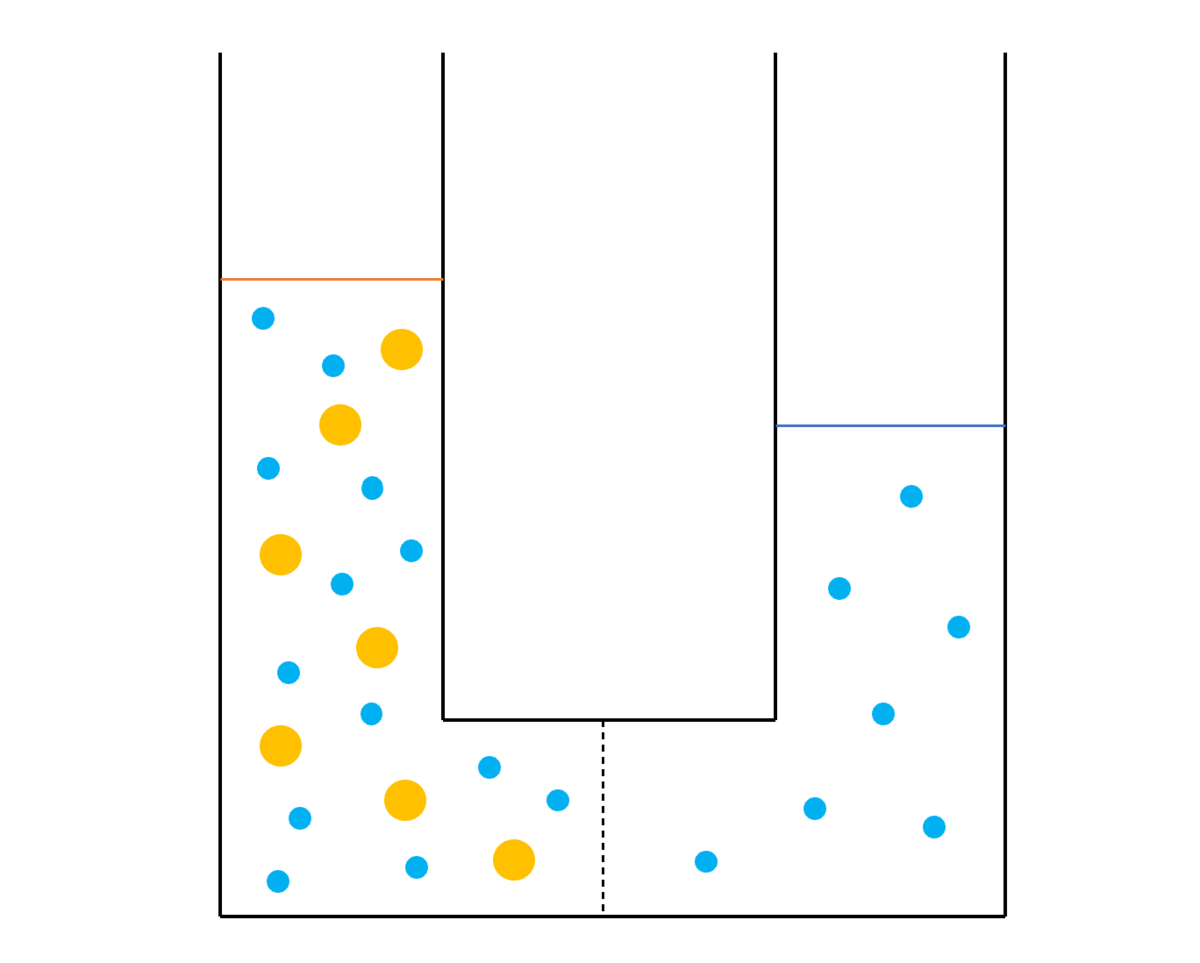
水分子が移動したことにより、純水の液面は下がり、水溶液に液面は上がります。
しかし、実際にこの状態のまま止まるということはありません。
ここで高さをそろえるために、水溶液の液面に力が加わります。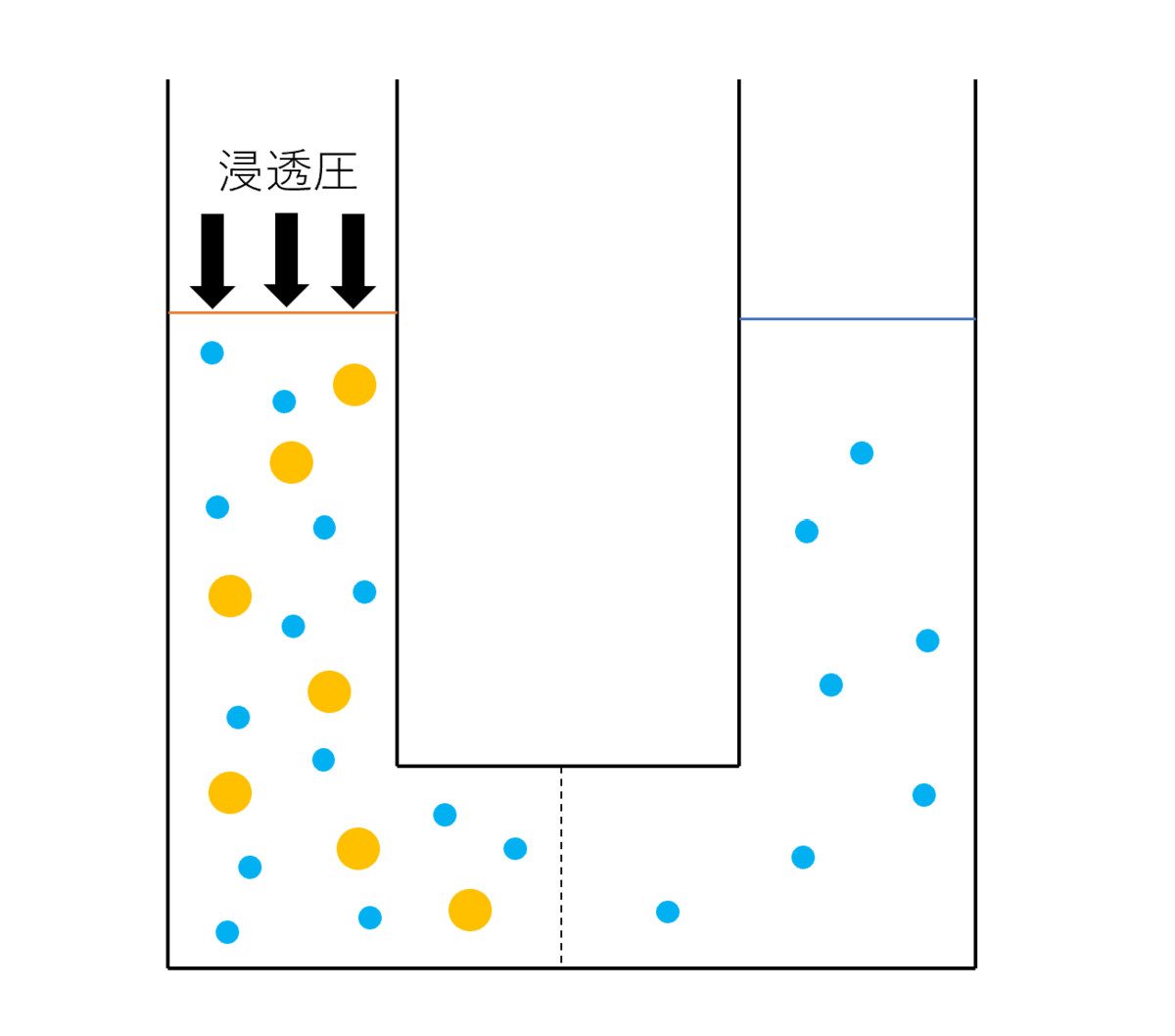
この時加えられた圧力のことを浸透圧と呼びます。
梅酒(ジュース)の場合
では梅酒の場合で考えてみましょう。
最初に梅と酒と氷砂糖を容器の中に入れます。
この段階では梅の中の方が濃いので、外側の酒が梅の皮を半透膜として、梅内部に向かって浸透していきます。
しばらく時間がたつと氷砂糖が解けていきますよね。
そうすると酒側の濃度が高くなります。
内部の梅の味が染みたおいしい液体が今度は外側に向かって染み出てきます。
これでおいしい梅酒の完成です。
これが氷砂糖ではなく普通の砂糖を使ってしまうと最初からお酒側の濃度が高くなってしまい、十分に梅の味が出てこないのです!
まとめ
このように科学の考え方が日常でも使われているというのはとても面白いですよね!
皆さんもこの暑い夏、梅ジュースを作りながら化学の勉強をしてみてはいかがでしょうか。
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
シャルルの法則とは何か【化学】【高校】
皆さんこんにちは!
今回はボイルの法則に続いて気体に共通する法則であるシャルルの法則について解説していこうと思います。
ボイルの法則については下の記事をご覧ください。
study-college-student.hatenablog.com
それでは今回も最初にシャルルの法則の形を見ておくことにしましょう。
もしくは
(は一定)
それではこの式は何を表しているのか見ていくことにしましょう!

定義
まずはシャルルの法則の定義から確認していきましょう。
「圧力一定の時、気体の体積Vは温度Tと比例の関係にある。」
ここで注意してほしいのは
○圧力が一定であるということ
○温度の単位が°Cではないということ
この二つです!
シャルルの法則について詳しく説明していく前に温度の単位について説明しておきます。
Cではない温度の単位と聞いてピンと来た人は少し飛ばして続きを読んでみてください。
絶対温度とは
化学の世界では温度の単位としてC(セルシウス温度)ではなく、絶対温度K(ケルビン)を使います。
この世の中の分子たちは人間と同様にエネルギーをもとに動き回っていますが、温度を下げていくことでこのエネルギーが徐々に小さくなっていきます。
いずれエネルギーがなくなるときの温度を絶対温度と呼び、これはCであるといわれています。
絶対温度はこの絶対零度を0Kとしたときの温度を表したものです。
つまりと定義されています。
これより温度の単位の変換はセルシウス温度t[C]を絶対温度T[K]にすると次のような式が成り立つということになります。
セルシウス温度に273を加えるだけです!
この273という数字をしっかり覚えておきましょう!
問:それぞれの温度を絶対温度に表せ。
(1) (2)
答え:
(1)300K (2)173K
それではシャルルの法則の話に戻っていきます。
シャルルの法則の意味
圧力が一定の時、体積と絶対温度が比例の関係にあるとはどういうことでしょうか。
比例ということですから
「絶対温度が2倍、3倍......となると体積も2倍、3倍......になる」
ということですね。
これは身近な現象でもあります。
例えば、「コンビニ弁当や袋に入ったパンを電子レンジで加熱した際に爆発した」という経験はありませんか?
まさにあれがシャルルの法則ですね。
加熱したことにより内部の気体の体積が膨張し爆発します。
(水蒸気による影響もあるとは思います。)
気体も目には見えないサイズの分子たちの運動です。
分子たちは熱をエネルギーとして活動をしています。
私たち人間がご飯をたべ、エネルギーにし活動をしているのと同じです。
絶対温度を上げ、エネルギーを受け取った分子たちは前よりも激しく運動をします。
それにより気体の体積が大きくなるのです。

では簡単な例題を見ていきましょう。
例題
問:圧力一定の条件で、で
を
まで加熱すると体積Vは何Lとなるか。
圧力一定なのでシャルルの法則を使うことができます。
今回の問題をよく見ると温度の単位が絶対温度ではありません。
ここに引っかからないように気を付けてください。
300Kから400Kに変化したということは倍になったということです。
よってシャルルの法則より、体積も倍になります。
したがって答えは、
まとめ
○シャルルの法則
「圧力一定の時、気体の体積と絶対温度は比例の関係」
○絶対温度
= t[^\circ C] + 273]
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
ボイルの法則とは?【化学】【高校】
皆さんこんにちは!
今回は高校化学気体の性質で習うボイルの法則とはいったい何なのかについて簡単に解説していこうと思います!
ボイルの法則の式は次のような式になります。
または
(は一定)
この式の意味と実際の使い方について理解していきましょうね!

ボイルの法則とは
まずは教科書に載っている定義から確認していきます。
定義
「温度一定の時、一定物質量の気体の体積Vは圧力Pに反比例する。」
この関係は1662年に発見されました。
これを式で表現すると、次のような式になります。
(
は一定)
この法則が表していることは何なのか、確認していきましょう!
法則の意味
圧力と体積が反比例する。
つまり、
圧力が大きくなればなるほど体積が小さくなる
ということですよね。
それでは下の図を見てみてください。
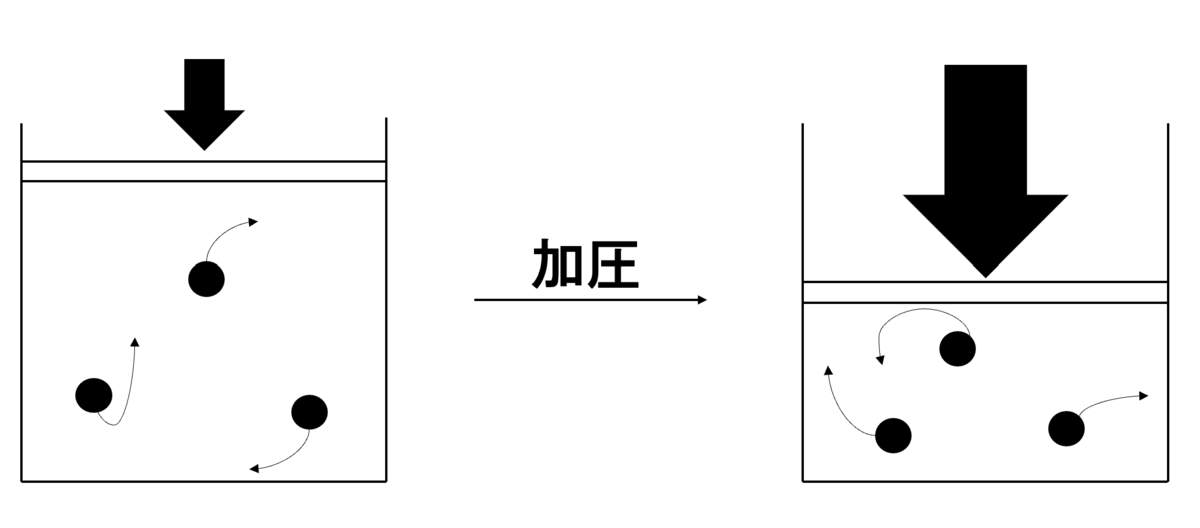
図のように気体が入った入れ物のふたの部分に強い力を加える(圧力を加える)と入れ物の中の気体の体積は小さくなりますよね。
これは普段生活している中でもよく起こっている現象で当たり前すぎるくらいだと思います。
ボイルの法則はこの当たり前の現象が、実は反比例の関係にあるということを言っているだけなのです!
(ただし、何でもいいというわけではなくて、温度一定の時のみ反比例という関係がなりたつということに注意してください。)
それでは少し例題を見て理解を深めていきましょう。
例題
問:温度一定で、圧力200Pa、体積5Lの気体の圧力を100Paにすると体積は何Lになるか。
この問題は、最初に温度一定と書いてありますよね。
これが書いてあるためにボイルの法則を使うことができます!
それではボイルの法則を適用して解いていきましょう。
反比例という言葉は小学校でも習いますが、
「一方の変数が2倍、3倍、4倍......となるともう一方は1/2倍、1/3倍、1/4倍......になる」という関係でした。
今回の問題では圧力が変化していますが、
200Paから100Paということで1/2倍となっています。
ということは、体積は2倍になります。
よって求める体積Vは
となります。
まとめ
ボイルの法則とはいったい何なのかについて理解していただけましたか?
あらためてまとめておくと、
○温度一定の時圧力と体積は反比例の関係にある
ということでしたね!
ボイルの法則は気体に関する法則の一種でほかにも法則があるのでそちらに関してはまた別の記事で書いていこうと思います。
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!
英語長文の勉強法【受験生】【勉強法】
皆さんこんにちは!
今回は自分が受験期に行っていた英語長文の勉強法について紹介していこうと思います。
この記事は下記事の続きとなっていますので先にそちらを読んでみてください!
study-college-student.hatenablog.com

結論
英語長文をより速く正確に読むために大切にしてほしいことは、
とにかく長文を読むたびに「構造分析」をするということです。
模試や参考書、赤本で長文を読むたびにその復習として構造分析をしていました。
そもそも構造分析とは何かといいますと、簡単に言えば、S(主語)V(動詞)O(目的語)C(補語)M (修飾語)を文中の単語一つ一つに振っていく作業のことです。
一文ずつ正確に構造をとらえていくという勉強法です。
ある程度の単語力、文法力を持っていても長文が解けないという人にはお勧めです。
構造分析をすることに慣れておくと試験本番で長文を読む際に、
「どれが主語でどれが目的語なんだろう?」などと考える時間少なくなります。
実際にいつどんな参考書を使っていたかをまとめていきます。
使用した参考書について
構造分析
「合格へ導く英語長文Rise」という参考書を一通り解くことで勉強しました。
この参考書は長文中によく出てくるさまざまな文構造についてまとめられており、それぞれに例題がついているため身につけた知識を速攻でアウトプットできるので知識が身につきやすくお勧めです。
時期としては長文学習を本格的に始める前にまずこれから始めるといいと思います。
長文問題集
①やっておきたい英語長文シリーズ
「無駄がない」といった感じの参考書です。一長文当たりの文字数に応じて300,500,700,1000と4段階で販売されています。
最初は自信がある人でも500から始めることをお勧めします。
解説にはパラグラフごとの和訳が書いてあるので復習がやりやすいというのもいい点ですね!
②イチから鍛える英語長文シリーズ
やっておきたいシリーズと似たような参考書になります。
こちらはBasic,300,500,700という4段階のレベル分けで販売されています。
やっておきたいシリーズとの違いはデザインが大きいと思います。
全編カラーでおしゃれなデザインとなっています(笑)
個人的には単調なデザインよりもやる気が出るのかなと思います。
どちらも良い長文しか収録されていないのでこれから長文の参考書を買おうかなと思っている人は一度書店で見てみてください!
これらを解き終わったら先に述べた「構造分析」をしてしっかり復習してくださいね!
まとめ
今回は英語長文の勉強で自分自身がやってきた勉強法について書いてみました。
とにかく構造分析をすることが大事ということです。
確実に力が付きます。
参考にしてみてくださいね!
こちらもあわせてどうぞ。
study-college-student.hatenablog.com
質問要望等は随時コメントで受け付けております。何かございましたらお気軽にご連絡ください!